Souhrn
Metabolismus kostí může být ovlivněn i konkomitantně užívanými léčivy, všechny léky ovlivňující metabolismus kostí mohou vyvolat hypokalcemii. Během terapie denosumabem je nutné zajistit dostatečný přísun jak vápníku, tak vitaminu D. Biologická dostupnost vápníku závisí na mnoha faktorech, totéž platí i pro prekurzory vitaminu D. Vápenaté soli potřebují pro dobré vstřebávání kyselé prostředí. Aktivní vstřebávání vápníku střevní sliznicí je účinné do dávky cca 500–600 mg elementárního kalcia, vápník je lépe vstřebatelný večer. Vitamin D lze podávat jak ve formě cholekalciferolu, tak již vytvořeného plně aktivního kalcitriolu, užít lze i různé mezistupně metabolismu cholekaciferolu. U rizikových pacientů je nutné nejen suplementovat vápník a vitamin D, ale také aktivně předcházet malnutrici, např. vhodnou nutriční intervencí.
Klíčová slova: denosumab, vápník, vitamin D, suplementace
Kost
Kost je zvláštní formou pojivové tkáně, složenou z kolagenní matrix impregnované mikroskopickými krystaly fosfátů vápníku, zejména ve formě hydroxyapatitů (Ca10(PO4)6(OH)2). Stará kost se neustále odbourává a tvoří se nová. Pro udržování normální kostní struktury jsou proto zapotřebí dostatečná množství proteinů a minerálů. Kostní buňky primárně zajišťující tvorbu a resorpci kosti jsou osteoblasty a osteoklasty. Osteoblasty (z řeckého blastos = zárodek) jsou buňky tvořící kost, jsou odvozené ze stromálních buněčných prekurzorů kostní dřeně a vytvářejí velká kvanta kolagenu I. typu. Tato kolagenní vlákna jsou následně mineralizována hydroxyapatitem a osteoblasty se diferencují v osteocyty.
Osteoklasty (z řeckého klastos = lámat) jsou mnohojaderné buňky erodující a resorbující dříve vytvořenou kost. Pocházejí z hematopoetických kmenových buněk a vznikají z monocytů, stejně jako např. Kupfferovy buňky v játrech. Upevňují se na kost, pomocí protonové pumpy okyselují místo kontaktu na pH 4. Kyselé pH rozpouští hydroxyapatit, proteázami se pak rozkládá kolagen, čímž se v kosti vytváří mělká deprese (resorpční lakuna). Produkty natrávení kosti pak přecházejí do intersticiální tekutiny, čímž se zvyšuje i hladina vápníku v krvi. Klíčovým mediátorem funkce, formace a přežívání osteoklastů je receptor aktivující nukleární faktor kappa B (RANK, ligand RANKL). Fyziologicky je tento proces blokován osteoprotegerinem, který vyváže RANKL dříve, než se dostane ke svému mateřskému receptoru, a nedojde tedy k plné aktivaci uvedené dráhy [1].

Tabulka č. 1: Příklady léčiv, která ovlivňují hladinu vápníku (Ca)
Zdroj: podle Liliams G, Milionis HJ, Elisaf M, 2009 [ 3]
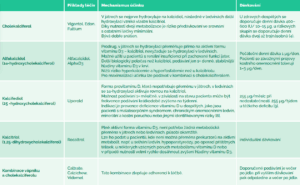
Kostní tkáň je v průběhu života stále přebudovávána podle potřeb těla, udržuje se stálá rovnováha mezi osteoblasty a osteoklasty. Metastázy různých nádorů tuto přirozenou rovnováhu významně narušují, porucha homeostázy kalcia tak patří k častým komplikacím maligních onemocnění. Setkat se můžeme jak s hyperkalcemií, např. při metastatické diseminaci karcinomu prsu, tak i s hypokalcemií. Příčiny hypokalcemie jsou mnohočetné; k obvyklým patří nedostatek kalcia ve stravě, jeho nedostatečná či porušená absorpce, zvýšená exkrece kalcia ledvinami, nedostatečný přísun vitaminů skupiny D, jejich porušený metabolismus či kombinace všech těchto faktorů. Metabolismus kostí může být ovlivněn i konkomitantně užívanými léčivy (tab. č. 1). Problematika terapie denosumabem a její vliv na metabolismus vápníku je i tématem tohoto sdělení [2].
Denosumab
Denosumab představuje první biologické léčivo určené k léčbě osteoporózy, které zasahuje do kaskády aktivace osteoklastů a následné osteoresorpce. Jedná se o lidskou monoklonální protilátku IgG2 primárně indikovanou pro léčbu osteoporózy, další indikace udává tabulka č. 2.
Denosumab je lidská monoklonální protilátka (IgG2), která se s vysokou afinitou i specificitou zaměřuje a váže na RANK a zabraňuje aktivaci jeho receptoru, inhibuje tvorbu a životnost osteoklastů, a tím snižuje resorpci kortikální a trabekulární kosti. Terapie denosumabem tak ovlivňuje metabolismus vápníku – zastavuje odbourávání kostí, což může vést k hypokalcemii. Rizika zvyšuje i preexistující deficit vitaminu D, který je u onkologických pacientů častý. Během terapie denosumabem je proto nutné zajistit dostatečný přísun jak vápníku, tak vitaminu D, což je uvedeno i v souhrnech údajů o přípravku (SPC) léčiv, která obsahují denosumab. Problém může nastat např. v situaci, kdy pacient trpící osteoporózou, bývá zaléčen podáváním vápníku a vitaminu D, po nasazení denosumabu se pak může mylně domnívat, že vápník a vitamin D již užívat nemusí, protože už dostal „opravdový“ lék. Tato domněnka je ovšem mylná a ve svém důsledku může pacienta významně ohrozit. U onkologických pacientů, zejména v paliativní péči, může docházet k vysazování suplementace vápníkem a vitaminem D ve snaze o minimalizaci medikace.
Vápník
Tělo dospělého člověka obsahuje přibližně 1 kg vápníku, přičemž 99 % vápníku je v kostře. Volné, ionizované kalcium je vitálně důležitým druhým poslem a je nezbytné pro srážení krve, svalovou kontrakci a pro funkci nervů. Pokles extracelulárního Ca2+ má in vivo zřetelný excitační účinek na buňky nervů a svalů. Následkem je hypokalcemická tetanie, charakterizovaná rozsáhlými spazmy kosterních svalů, postihujícími zejména svaly končetin a laryngu.

Tabulka č. 2: Léčiva obsahující denosumab
Zdroj: podle SPC zmíněných přípravků
Příjem vápníku potravou
Doporučený denní příjem vápníku je závislý na věku a pohlaví, mírně se liší podle různých zdrojů (FAO, WHO, EFSA). Zjednodušeně se dá říci, že minimální denní příjem pro dospělého by měl být 1 g vápníku [4]. Chceme-li zajistit příjem dostatečného množství vápníku potravou, je vhodné doporučenou dávku rozdělit do více porcí s obsahem 200−250 mg vápníku na porci. Taková porce je potom cca 200 ml mléka, 30 g sýra, 150 ml jogurtu, 60 g sardinek, 500 g listové zeleniny, 200 g ořechů či 600 g pomerančů [5]. Ukázka jídelníčku pro pacienta s dietou 1 200 mg vápníku/den, je uvedena v tabulce č. 3.

Tabulka č. 3: Ukázka jídelníčku pro pacienta s dietou 1 200 mg vápníku/den
Zdroj: podle Svačina Š. a kol., 2008 [5]
Je těžko představitelné, že by onkologičtí pacienti byli schopni tuto dietu dlouhodobě dodržovat, ať už z důvodů finančních, organizačních i vlivem vlastního onemocnění. Další otázkou je míra využití vápníku z potravin, která závisí na hodnotách pH v tenkém střevě – alkalické hodnoty vstřebávání vápníku snižují. Vstřebávání vápníku ovlivňuje i množství vitaminu D, přítomnost fytátů (např. z cereálií), šťavelanů (špenát), fosfátů (tavené sýry, měkké uzeniny, colové nápoje apod.) a mnoha dalších faktorech. K zamyšlení vede první uvedená podmínka, tedy hodnota pH ve střevě. Značné množství pacientů dlouhodobě užívá inhibitory protonové pumpy (PPIs), nedostatečnou tvorbou kyseliny chlorovodíkové v žaludku se logicky zvyšuje pH tráveniny i v duodenu. Díky tomu se snižuje biologická dostupnost vápníku (i hořčíku), na což upozorňují i souhrny údajů o přípravku (SPC) léčivých přípravků obsahujících PPIs. Zajištění dostatečného množství vápníku u pacientů užívajících PPIs je tedy poměrně náročné.
Nedostatečný příjem vápníku potravou a jeho snížená biologická dostupnost vedou v praxi k nutnosti vápník suplementovat farmakologicky. K dispozici jsou uhličitan vápenatý (CaCO3) a vápenaté soli kyseliny glukonové, mléčné a citronové. S výjimkou citrátů potřebují pro dobré vstřebávání všechny tyto soli kyselé prostředí, chronické užívání antacid, inhibitorů protonové pumpy, popř. H2 blokátorů, tak významně snižuje biologickou dostupnost vápníku i v této formě. Při nutnosti užívat tato léčiva a zároveň suplementovat vápník je vhodné zvýšit kyselost žaludečního obsahu, např. zapíjet vápenatou sůl kyselými nápoji.
Dalším důležitým faktorem úspěšnosti suplementace kalcia je jeho dávkování. Aktivní vstřebávání vápníku střevní sliznicí je účinné do dávky cca 500–600 mg elementárního kalcia. Větší jednorázová dávka nezvýší množství využitelného vápníku, v případě nutnosti podávat vyšší dávky je tak vhodné dávku rozdělit. Vápník je vhodné podávat s jídlem, nejlepší vstřebatelnost je večer před ulehnutím, protože se pak snižuje noční vrchol koncentrace parathormonu v krvi [6].
U malnutričních pacientů suplementace samotného vápníku často nestačí. V metabolismu kosti hraje významnou roli i hořčík, který se funkčně podílí na konverzi vitaminu D na aktivní formu a ovlivňuje produkci a uvolňování parathormonu. Kombinace nízké hladiny vápníku a nízké hladiny hořčíku v krvi je pouhou suplementací vápníku špatně ovlivnitelná, zejména za současného deficitu vitaminu D [4]. K situaci, kdy pacient trpí nedostatkem jak vápníku, tak hořčíku, opět přispívá i užívání inhibitorů protonové pumpy (PPIs). Inhibitory protonové pumpy, stejně jako diuretika, významně inhibují kanál TRPM6/7, který řídí absorpci magnezia a kalcia na úrovni enterocytu a jejich eliminaci tubulárními epiteliemi ledvin – diuretika na úrovni nefronu, inhibitory protonové pumpy na úrovni ledvin a na úrovni enterocytu. Léčba PPIs tak může vést k významné depleci vápníku i hořčíku a nutnosti suplementovat oba tyto ionty [7].
Vápník a hořčík používají stejné transportní mechanismy, při současném podávání dochází ke kompetici o tyto transportní systémy, a snižuje se tak biologická dostupnost obou prvků, souběžné podávání tedy nedává smysl a je vhodné užívat tyto přípravky odděleně, hořčík ráno a vápník večer [4].
Vitamin D
Deficit vitaminu D je u onkologických pacientů častý, existuje zde řada důvodů k jeho nedostatku – strava s nízkým obsahem živočišných, mléčných tuků a/nebo jejich mal-absorpce, malnutrice, nízká expozice slunečnímu světlu, užívání krémů na opalování (od ochranného faktoru 8 výše brání konverzi vitaminu D v kůži). Problémem je i nedostatečná metabolická konverze prekurzorů kalcitriolu na aktivní formy při postižení jater a ledvin (tab. č. 4), případně narušení metabolismu vitaminu D konkomitantní medikací (tab. č. 1).
Zjednodušeně lze říci, že primární prekurzor – dehydrocholesterol – je UV zářením přeměněn na cholekalciferol. Takto získaný provitamin je neaktivní, aktivuje se dvoustupňovou hydroxylací na 25. uhlíku (v játrech) a na 1. uhlíku (v ledvinách). Vitamin D můžeme pacientovi podávat jak ve formě cholekalciferolu, tak již vytvořeného plně aktivního kalcitriolu. Užít lze i různé mezistupně metabolismu cholekaciferolu jako je 1α-hydroxycholekalciferol, který je již hydroxylován na prvním uhlíku a stačí mu hydroxylace v játrech, nebo 25-hydroxycholekalciferol, kde již proběhla aktivace 25. uhlíku (tab. č. 5).
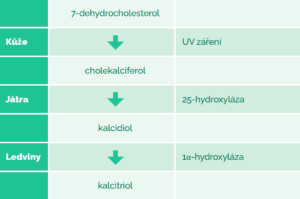
Tabulka č. 4: Vznik vitaminu D
Zdroj: podle Ganong WF, 2001 [1]
Vitamin D patří k vitaminům rozpustným v tuku, je tak vhodné jeho podávání současně s jídlem obsahujícím tuky – plnotučný jogurt, chleba s máslem apod. Porucha vstřebávání vitaminu D může nastat i u malabsorpcí tuku, např. onemocnění žlučníku, pankreatu, celiakie, případně současného deficitu dalších vitaminů nebo stopových prvků – zejména vitaminu K nebo hořčíku. U zdravých dospělých se doporučuje denní dávka cholekaciferolu 400–600 IU/ 10–15 μg, u rizikových skupin se doporučuje denní dávka dvoj- až trojnásobná [4]. Podávání již aktivovaných forem vitaminu D je určeno pro léčebné, nikoliv preventivní užití.
Tabulka č. 5: Suplementace vitaminu D
Zdroj: není-li uvedeno jinak, podle SPC zmíněných přípravků

Tabulka č. 6: Příklady potravin pro zvláštní lékařské účely určené při riziku podvýživy u onkologických pacientů
Zdroj: podle SPC příbalových letáků zmíněných přípravků
Bílkoviny
Základní stavební jednotkou kolagenu jsou aminokyseliny, kvalita a kvantita bílkovin v organismu tak hrají významnou roli i v metabolismu kostí. U rizikových pacientů je tak nutné nejen suplementovat vápník a vitamin D, ale také aktivně předcházet malnutrici, např. nutriční intervencí. Ke zvážení je tak užití nutriční podpory, zejména enterální výživy k popíjení, která je pro onkologické pacienty obohacena nejen omega-3 mastnými kyselinami, ale obsahuje i vápník a vitamin D (tab. č. 6). Důležitým faktorem je také přiměřený pohybový režim, vhodná zátěž kostí a dostatečná svalová síla.
Závěr
Všechny léky ovlivňující metabolismus kostí mohou vyvolat hypokalcemii. Při léčbě denosumabem je riziko hypokalcemie vyšší než při léčbě bisfosfonáty, rizikoví jsou zejména pacienti s renální insuficiencí. Před zahájením léčby je proto třeba upravit preexistující nedostatek vápníku a hladinu kalcia je třeba v průběhu léčby kontrolovat. Současně s podáváním denosumabu je doporučováno podávat kalcium (500 mg až 1 g/den) a cholekalciferol (400–800 IU/den), popř. odpovídající dávky jiných prekurzorů vitaminu D [10].
Při suplementaci vápníkem je třeba vzít v potaz skutečnost, že vápenaté soli potřebují pro dobré vstřebávání kyselé prostředí, respektovat, že aktivní vstřebávání vápníku střevní sliznicí je účinné do dávky cca 500–600 mg elementárního kalcia i skutečnost, že vápník je lépe vstřebatelný večer. Biologickou dostupnost snižují další soli užívající stejné transportní mechanismy, např. hořčík nebo zinek, významný vliv hraje konkomitantní užívání inhibitorů protonové pumpy. Vitamin D je třeba užívat současně s jídlem obsahujícím tuk. Limitující faktory vstřebatelnosti prekurzorů vitaminu D jsou hypomagnezemie a nedostatek vitaminu K, případně další medikace, zejména alterující ledvinné funkce. U rizikových pacientů je nutné nejen suplementovat vápník a vitamin D, ale také aktivně předcházet malnutrici, např. vhodnou nutriční intervencí.
PharmDr. MVDr. Vilma Vranová, Ph.D.
PharmDr. Karel Vašut, Ph.D.
Ústav aplikované farmacie FAF MUNI Brno
Zdroj: časopis Podpůrná léčba č. 3/2025, ISSN (TIŠTĚNÉ VYDÁNÍ): 2571-2438, ISSN (ONLINE VYDÁNÍ): 2694-7269 registrováno pod evidenčním číslem MK ČR E 23500
LITERATURA
1. Ganong WF. Přehled lékařské fyziologie. Praha: Galen, 2001.
2. Rampulová I, Dubská L, Votavová I, et al. Hypokalcemie u onkologických pacientů – existuje souvislost s nedostatkem cholekalciferolu [online]? XXII. brněnské onkologické dny dostupné z https://www.linkos.cz/lekar-a-multidisciplinarni-tym/kongresy/po-kongresu/databaze-tuzemskych-onkologickych-konferencnich-abstrakt/hypokalcemie-u-onkologickych-pacientu-existuje-souvislost-s-nedostatkem-cholekal/ [cit. 1. 2. 2025]
3. Liamis G, Milionis HJ, Elisaf M. A review of drug-induced hypocalcemia.
J Bone Miner Metab. 2009; 27(6): 635–642.
4. Kohout P, Havel E, Matějovič M, et al. Klinická výživa. Praha: Galén, 2021.
5. Svačina Š a kol. Klinická dietologie. Praha: Grada, 2008.
6. Pavelka K, Vencovský J, Horák P a kol. Revmatologie. Praha: Maxdorf, 2018.
7. Vranová, V. Interakce léčiv u onkologických pacientů I. Podpůrná léčba. 2024; 6(2): 6–9.
Číslo schválení: PON-CZ-00002


